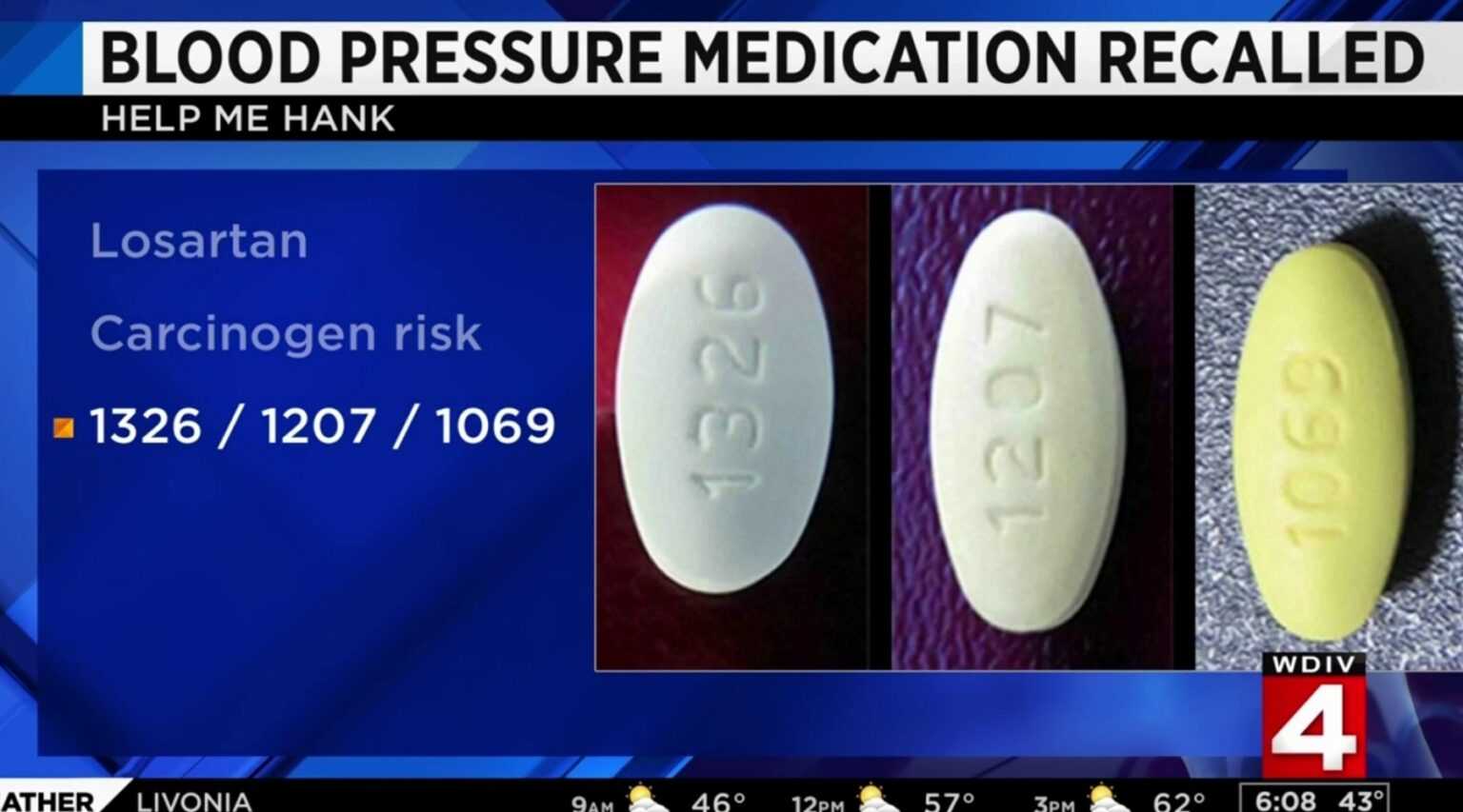
HΠΑ FDA: Ο FDA έκανε την αξιολόγηση του προϊόντος Lupine Pharmaceuticals μετά από εργαστηριακές δοκιμές Ένα φάρμακο για την αρτηριακή πίεση Lupine Pharmaceuticals Inc. ανακαλείται από την Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) επειδή περιέχει πιθανώς “καρκινογόνο για τον άνθρωπο”. Η εθελοντική ανάκληση περιλαμβάνει τα δισκία Irbesartan της εταιρείας και τα δισκία Hydrochlorothiazide σε επίπεδο καταναλωτή.

Σε ανακοίνωση της 14ης Οκτωβρίου, ο Οργανισμός είπε ότι έκανε την αξιολόγηση με βάση τα αποτελέσματα εργαστηριακών δοκιμών. “Στο πλαίσιο της συνεχιζόμενης αξιολόγησης του Lupin, η ανάλυση αποκάλυψε ότι ορισμένες δοκιμασμένες παρτίδες API (αλλά όχι παρτίδες τελικών προϊόντων) ήταν πάνω από το όριο προδιαγραφών για την ακαθαρσία, N-nitrosoirbesartan”, έγραψε ο FDA.
“Παρόλο που η Lupine δεν έχει λάβει αναφορές για ασθένειες που φαίνεται να σχετίζονται με αυτό το ζήτημα, η εταιρεία, από πολλή προσοχή, ανακαλεί όλες τις παρτίδες Irbesartan Tablets USP 75mg, 150mg και 300mg και Irbesartan και Hydrochlorothiazide Tablets USP, 150mg/12.5 mg και 300 mg/12,5 mg στις ΗΠΑ ». Η Lupine Pharmaceuticals, Inc. εκδίδει εθελοντικά πανεθνικά ανάκληση όλων των δισκίων Irbesartan και των δισκίων Irbesartan και υδροχλωροθειαζίδης λόγω πιθανής παρουσίας ακαθαρσιών Ν-νιτροζοϊρβεσαρτάνης
Η Lupine Pharmaceuticals, Inc. εκδίδει εθελοντικά πανεθνικά ανάκληση όλων των δισκίων Irbesartan και των δισκίων Irbesartan και υδροχλωροθειαζίδης λόγω πιθανής παρουσίας προσμίξεων Ν-νιτροζοϊρβεσαρτάνης (FDA)
Η διοίκηση σημείωσε ότι η Lupine Pharmaceuticals διέκοψε την εμπορία των καρτελών Irbesartan και Irbesartan και HCTZ τον Ιανουάριο. Από τον Οκτώβριο του 2018 έως τις 30 Σεπτεμβρίου 2021, η Lupine Pharmaceuticals φέρεται να έλαβε τέσσερις αναφορές ασθένειας από το Irbesartan και μηδενικές αναφορές από την Irbesartan και την υδροχλωροθειαζίδη. Τα δισκία Irbesartan USP 75mg, 150mg και 300mg συσκευάζονται σε φιάλες 30 και 90 τεμαχίων και διανέμονται σε χονδρεμπόρους, αλυσίδες φαρμάκων, φαρμακεία ταχυδρομικής παραγγελίας και σούπερ μάρκετ πανεθνικά. “Το Irbesartan Tablet USP είναι ένας αποκλειστής υποδοχέων αγγειοτενσίνης ΙΙ που ενδείκνυται για τη θεραπεία της υπέρτασης, για τη μείωση της αρτηριακής πίεσης, τη διαβητική νεφροπάθεια σε υπερτασικούς ασθενείς με διαβήτη τύπου 2, αυξημένη κρεατινίνη ορού και πρωτεϊνουρία”, εξήγησε ο FDA.
Τα δισκία Irbesartan και Hydrochlorothiazide USP, 150mg/12.5mg και 300mg/12.5mg συσκευάστηκαν επίσης σε φιάλες 30 και 90 τεμαχίων και διανεμήθηκαν σε χονδρεμπόρους, αλυσίδες φαρμάκων, φαρμακεία ταχυδρομείου και σούπερ μάρκετ σε όλη τη χώρα.
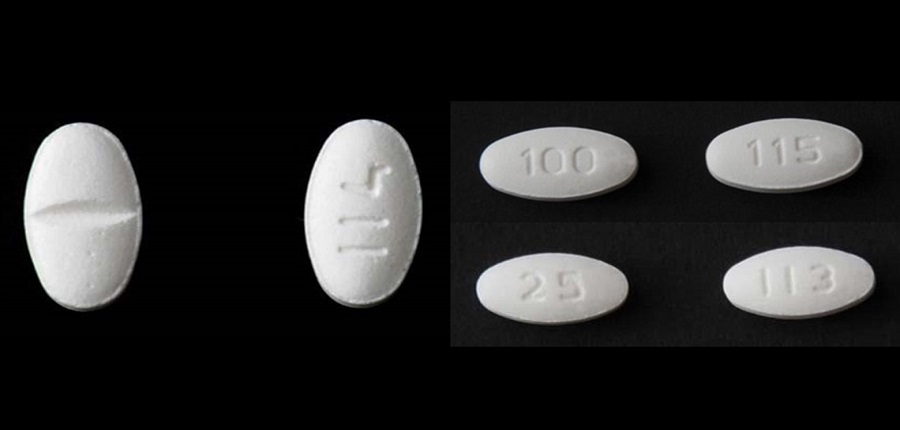
Σύμφωνα με τον FDA, η Lupine Pharmaceuticals ειδοποιεί τους χονδρεμπόρους, τους διανομείς, τις αλυσίδες φαρμάκων, τα φαρμακεία και τα σούπερ μάρκετ μέσω τηλεφώνου και μέσω ειδοποίησης ανάκλησης, καθώς και την επιστροφή όλων των παρτίδων ανακληθέντων προϊόντων.
Η ειδοποίηση ανάκλησης συνέστησε ότι οι ασθενείς που λαμβάνουν δισκία Irbesartan USP, 75mg, 150mg και 300mg και Irbesartan και Hydrochlorothiazide USP, 150mg/12.5mg και 300mg/12.5mg θα πρέπει να συνεχίσουν να το κάνουν και να επικοινωνούν με τον φαρμακοποιό, τον γιατρό ή τον ιατρό τους για πληροφορίες σχετικά με εναλλακτικές λύσεις θεραπείας. Οποιεσδήποτε ανεπιθύμητες αντιδράσεις ή προβλήματα ποιότητας που αντιμετωπίζονται με τη χρήση αυτού του προϊόντος μπορούν να αναφερθούν στο πρόγραμμα Αναφοράς Ανεπιθύμητων Συμβάντων του MedWatch του FDA είτε online είτε με συνηθισμένο ταχυδρομείο ή φαξ.
Οι καταναλωτές, οι χονδρέμποροι, οι διανομείς ή οι λιανοπωλητές με ερωτήσεις σχετικά με την ανάκληση θα πρέπει να επικοινωνήσουν με την Inmar Rx Solutions Inc. στο (855) 769-3988 / (855) 769-3989 και οι ανακληθείσες παρτίδες θα πρέπει να επιστραφούν στην Inmar Rx Solutions Inc. για επιστροφή χρημάτων. Ο αριθμός της παρτίδας βρίσκεται στο πλάι της ετικέτας της φιάλης.